「酸性で無色、塩基性でピンク」。覚えるのは簡単。
でも本当は、分子の“形の比率”が平衡で入れ替わって、光の吸い方が変わる話。
結論
色は「どの形が多いか」で決まる。
フェノールフタレインは弱酸としてふるまい、pHによって分子種(形)が変わります。
低pHでは無色の形が多く、pHが上がると脱プロトン化した有色の形が増えるため、ピンクに見えます。
指示薬としての色変化域(だいたい pH 8.2〜10)は、「無色形」と「有色形」の比が一気に入れ替わる領域です。
数字を丸暗記するより、平衡で比率が動く、という骨組みを持つと強いです。
さらに強い塩基性では、別の無色形へゆっくり変わって退色することもあるので、
「塩基性ならずっとピンク」とだけ覚えると実験で混乱しやすいです。
あるある
「そういうもの」で覚えて、理由が手元に残らない。
実験レポートだと「ピンクになった→塩基性」と書いて終わってしまいがち。
でも口頭で「なんで?」と聞かれた瞬間、手が止まるやつです。
シママ、今日ちょっと引っかかっとる顔たい。
ねぇ、フェノールフタレインの色が変わる理由ってなんなんだろう?塩基性だから、とかじゃなくて、もっとこう、何かが“つながってない”気がするのよ。
なるほどたい。”つながる”ためには色の物理と化学平衡の概念が必要やね。
まず“色って何?”から始めて、最後に平衡へ着地させるばい。
それ助かる…。平衡って言われると、式だけ出てきて置いていかれる感じがするのよ。
本文
色は現象。理由は「比率が動く」こと。
1) まず「色」は、光の吸い方の結果
分子が可視光のどこかを吸収すると、残った光が目に届いて「色」に見えます。
吸収がほとんど可視に無ければ無色に見え、吸収の位置が変われば見える色も変わります。
2) 次に「構造」:pHで“形”が切り替わると、吸収が変わる
フェノールフタレインは pH に応じて分子の形が切り替わります。
重要なのは、形が変わると、電子の広がり(共役)の長さが変わり、可視光を吸うかどうかが変わることです。
まず、酸性〜中性で主役になりやすいのが「ラクトン環が閉じた形」です。
この形は共役が短く、可視光を強く吸いにくいので、見た目は無色に寄ります。
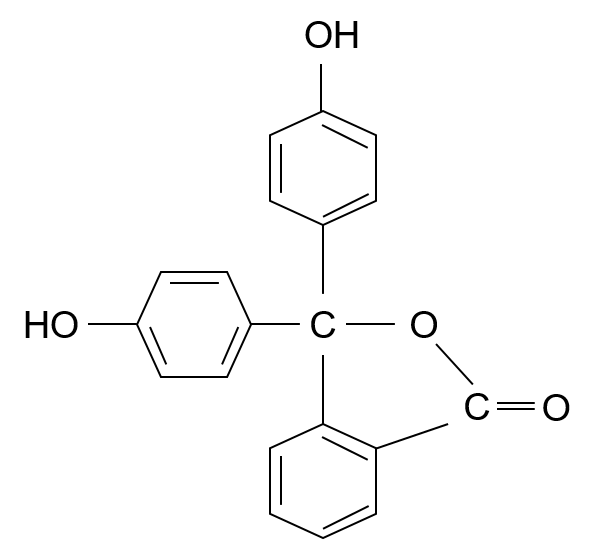
一方、塩基性側へ行くと脱プロトン化が進み、
「環が開いて共役が伸びた(キノノイド的な)形」が増えます。
共役が伸びると吸収が可視域へ寄り、結果としてピンクが見えるようになります。
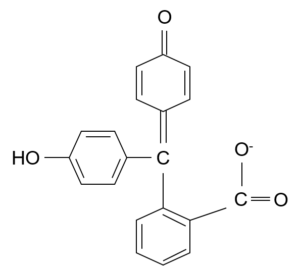
まずはこの2枚たい。無色側(閉環)と有色側(開環)を見分けられたら、
あとは「どっちが多いか」だけの話になるばい。
なるほど…。今まで“色だけ”見てたけど、
「閉環だと無色寄り」「開環で共役が伸びるとピンク」って、構造で言えるのね。
3) 本体は「平衡」:無色形と有色形の比が pH で動く
ここからが「色=平衡」の接続です。
どちらの形も“存在できる”だけでは色は決まりません。
溶液中でどちらが何割いるかで、見える色が決まります。
指示薬として抽象化すると、無色の酸型を $\mathrm{HIn}$、有色の塩基型を $\mathrm{In^-}$ として
$$\mathrm{HIn \rightleftharpoons H^+ + In^-}$$
という酸解離平衡で捉えられます。比率はヘンダーソン–ハッセルバルヒ式で一行です:
$$\mathrm{pH} = \mathrm{p}K_a + \log\left(\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]}\right)$$
pHが上がるほど $\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]}$ が増え、有色形の比率が増える。
これが「塩基性でピンクになる」の正体です。
“比率が増える”って言われても、まだピンと来ないのよね。
どれくらい増えたら、見た目が変わるの?
そこたい。じゃあ計算例を一個だけやるばい。
“pHが1動くと比が10倍動く”って掴めたら、色の切り替えが腹に落ちる。
4) 計算例:pHが1上がると、比は10倍変わる
ここでは色変化域の中心として、代表値の $\mathrm{p}K_a \approx 9.5$ を使って
「比の動き方」だけを見ます(実際のフェノールフタレインは複数段の平衡を持ちますが、
“色のスイッチ”の感覚づくりにはこの近似が効きます)。
条件:$\mathrm{p}K_a = 9.5$ として、pH 8.5 と 9.5 を比べる
(A)pH = 8.5 のとき
$$8.5 = 9.5 + \log\left(\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]}\right)$$
$$\log\left(\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]}\right) = -1.0$$
$$\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]} = 10^{-1} = 0.1$$
有色形は無色形の 0.1倍。無色が主役なので、見た目はほぼ無色(またはごく薄い)。
(B)pH = 9.5 のとき
$$9.5 = 9.5 + \log\left(\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]}\right)$$
$$\log\left(\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]}\right) = 0$$
$$\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]} = 1$$
有色形と無色形が同じくらい。ここから上で「ピンクが勝ち始める」。
つまり、pHが1上がるだけで比が10倍動く。だから変色は“じわじわ”ではなく、見た目として一気に切り替わります。
5) もう一段:強塩基で退色するのは「別の形」へ寄るから
フェノールフタレインは、弱塩基性でピンクになったあと、
さらに強い塩基性では別の無色形へ変化して退色することがあります。
だから条件によっては「塩基性のはずなのに無色」が起こり得ます。
ここでも考え方は同じで、「平衡で主役が移った」と捉えればOKです。
色は“比率”の結果なので、比率の主役が無色側へ寄れば、見た目も無色へ戻ります。
テンプレ
指示薬の説明は、この順番で崩れない。
(1)色の正体
「色は可視光の吸収の違い」
(2)構造の切り替え
「pHで分子種(形)が変わり、吸収が変わる(閉環↔開環)」
(3)平衡で比率が決まる
$$\mathrm{HIn \rightleftharpoons H^+ + In^-}$$
$$\mathrm{pH} = \mathrm{p}K_a + \log\left(\frac{[\mathrm{In^-}]}{[\mathrm{HIn}]}\right)$$
(4)一言でまとめる
「pHで比率が入れ替わるから、色が切り替わる」
落とし穴
色だけで、強さまで断定してしまう。
落とし穴は一つ。「ピンク=塩基性」から先を全部決め打ちすることです。
フェノールフタレインは“ピンクになる窓”があって、その外側では無色の形が主役になることがあります。
色は便利だけど、理屈を持たないと条件で転びます。
締め
暗記を、理論に置き換える。
今日のゴールは「ピンクになる」じゃなくて、
「なぜピンクに見えるかを、構造と平衡で言える」やったけんね。
図1(閉環)と図2(開環)を見分けられたら、もう半分勝ちたい。
うん、完全に納得。
もう「酸性で無色、塩基性でピンク」って暗記だけで持つんじゃなくて、
“閉環と開環のどっちが平衡で主役か”って、理論で説明できるのよ。
よかね。これで誰かに聞かれても、シママはもう“暗記の顔”にならんで済むたい。
逃げる前提で言うのやめなさいよ……。
でも今日は本当に、暗記じゃなくて理論で理解できた。ありがとう。