“100℃”の派手さに引っ張られがちだけど、鍵はそこじゃない。
反応熱 → 沸騰(相変化) → 圧力 → 噴射、という変換の流れを分解して見る。
結論
“熱い”の正体は、反応と相変化と圧力のセット。
ミイデラゴミムシ(いわゆるヘッピリ虫)の防御噴射は、
体内で別々に蓄えた成分を小さな反応室で混合し、酵素の助けで急速に反応させて発熱とガス生成を起こし、
そこで生じた高温の液滴・蒸気と刺激性物質(キノン類など)を外へ噴射する仕組みです。
よく知られる「約100℃」という表現は、古典的研究や解説で繰り返し引用される一方、
ミクロな二相噴射の温度を“どの位置の、どの相の、どの瞬間”で定義するかで値が揺れやすく、
数字だけが独り歩きしがちです。ここは断言よりも、「沸騰・蒸気を伴う高温が成立していること」を核に置くと、
説明が崩れません。
工学的な読み方は一本で、反応で出る熱量 $Q$ が、液体の顕熱と蒸発潜熱に割り当てられ、
生成ガスと蒸気で圧力が立ち、ノズル(狭い流路)で流速に変換されるというエネルギー変換として捉えます。
「すごい虫」ではなく、短時間・局所で相変化を絡めて圧力を作る“小型リアクタ+スプレーノズル”として見るのがいちばん分かりやすい。
あるある
数字だけに反応して、場所と時間が消える。
「100℃ってことは体内ぜんぶが100℃?」「お尻の中で爆発してるの?」みたいに、
温度の数字だけが先に走ってしまうやつ。ここを落ち着かせるだけで、理解が一段ラクになります。
シマナ、今日ちょっと静かたいね。何か考えごとしよる?
うん。技術の話って、派手な数字だけが切り取られると、急に嘘っぽく見えるのよ。
“説明の型”がないと、読者も置いていかれるでしょ。
じゃあ、型の練習にちょうどよか題材があるばい。摂氏100℃のオナラをする虫の話、聞く?
もう、そういう言い方するから話が軽くなるのよ……。
でも、題材としては確かに強いわね。“100℃”の独り歩き問題そのものだし。
まずはルールたい。「どこが」「いつ」「何が」。
温度は最後に置いて、反応室(局所)と噴射(外部)ば分けて見るけんね。
いい入り方。じゃあ本題。“100℃”は置いといて、仕組みを分解していきましょ。
本文
反応室(局所)で熱を作り、相変化で圧力に変え、噴射で仕事にする。
1) まず「どこが熱いか」:体全体じゃなく“反応室”
温度の話が荒れる最大の理由は、「噴射が熱い」=「体内ぜんぶが熱い」という短絡です。
実際には、反応が起きるのは腹部末端の反応室(チャンバー)で、
そこに貯蔵室(リザーバ)から必要な量だけが供給されます。
反応室は“混ぜる場所”、貯蔵室は“保管する場所”。役割分担があるから、成立します。
さらに重要なのは時間軸です。噴射は短時間に起き、外に出た瞬間から外気と混ざって急冷されます。
つまり「熱いかどうか」を語るなら、本当は
(反応室内の液相)と(噴射直後の二相流)と(空中で拡散した後)は分けて考える必要があります。
ここを分けた瞬間に、“数字の議論”が落ち着きます。
2) 何が反応しているか:見取り図を1枚入れる
防御液の詳細は種によって差がありますが、説明としては
「還元性の成分(ヒドロキノン系)+ 酸化剤(過酸化水素) → 酸化生成物(キノン類)+ 水」
という発熱する酸化反応として捉えると、工学の話に落としやすいです。
下の図は、その“代表式”のイメージです(実系は水溶液・混合物で、反応は段階的になり得ます)。
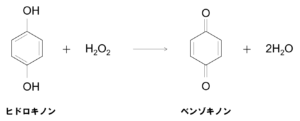
ここでは「熱が出る」「水が増える」「(別経路で)酸素が出る可能性がある」という三点が重要。
ここでのポイントは「何ができるか」よりも、「熱が出る」「(結果として)蒸気とガスが増える」の二点です。
熱は相変化(蒸気化)へ、ガスと蒸気は圧力へ、そして最後に噴射(運動エネルギー)へ変換される。
工学の言葉で言えば、反応(化学)→相変化(熱)→流動(機械)の連結です。
図があると早かろ。反応は「熱を出す」ための仕掛けたい。
そこから先は、熱が“蒸気と圧力”に化ける。
最初からそれを見せなさいよ……。
でも確かに、これなら「何が熱源か」が一発で分かるわね。
3) 「100℃」の扱い方:温度は“定義”が先、数字は後
「100℃」という表現は有名ですが、二相の微小噴射では温度測定が難しく、
測り方(位置・応答速度・接触/非接触)で観測値は変わり得ます。
だから本記事では、数字を“絶対の真実”として固定せず、
(沸騰・蒸気を伴う高温が成立している)という現象側を核に置きます。
この置き方なら、条件で温度が多少揺れても、説明が崩れません。
4) 熱力学の核:反応熱 $Q$ は、まず“沸点の壁”にぶつかる
反応室内の液体(水が多い混合液とみなす)に対して、発生熱 $Q$ が入ると、
まず温度が上がって沸点 $T_b$ に近づきます。
そこから先は、温度を上げるよりも蒸発(潜熱)に熱が吸われやすくなる。
ここが“高温噴射”と相性がいいところです。
断熱に近い(外へ逃げる熱を無視する)粗い近似なら、収支はこう書けます:
$$Q \approx m\,c_p\,(T_b – T_0) + m_v\,L_v$$
5) 実際の計算例:必要な熱量と、必要な反応量をざっくり出す
ここでは「どれくらいの熱で、どれくらいの蒸気が作れるか」を一回だけ手計算します。
ミクロ現象なので条件は仮定ですが、オーダー(桁)を掴むのが目的です。
仮定
・反応室の混合液の主成分を水として、質量 $m=10\ \mathrm{mg}=0.010\ \mathrm{g}$
・初期温度 $T_0=25^\circ\mathrm{C}$、沸点 $T_b=100^\circ\mathrm{C}$
・水の比熱 $c_p \approx 4.18\ \mathrm{J\ g^{-1}\ K^{-1}}$
・蒸発させる水の質量 $m_v=1\ \mathrm{mg}=0.001\ \mathrm{g}$
・水の蒸発潜熱 $L_v \approx 2257\ \mathrm{J\ g^{-1}}$
・(発熱反応の代表として)過酸化水素分解の反応熱 $|\Delta H| \approx 98\ \mathrm{kJ\ mol^{-1}}$($\mathrm{H_2O_2}$ 1 mol あたりの近似)
(1)25℃→100℃まで温める顕熱
$$Q_\mathrm{sens} = m\,c_p\,(T_b-T_0)$$
$$= 0.010\times 4.18 \times (100-25)$$
$$= 0.010\times 4.18 \times 75 \approx 3.14\ \mathrm{J}$$
(2)1 mgを蒸発させる潜熱
$$Q_\mathrm{vap} = m_v\,L_v = 0.001\times 2257 \approx 2.26\ \mathrm{J}$$
(3)必要な総熱量(ざっくり)
$$Q \approx Q_\mathrm{sens}+Q_\mathrm{vap} \approx 3.14 + 2.26 = 5.40\ \mathrm{J}$$
(4)この熱量を反応熱で賄うには?($\mathrm{H_2O_2}$分解で近似)
$$n(\mathrm{H_2O_2}) \approx \frac{Q}{|\Delta H|} = \frac{5.40\ \mathrm{J}}{98\,000\ \mathrm{J\ mol^{-1}}} \approx 5.5\times 10^{-5}\ \mathrm{mol}$$
$$m(\mathrm{H_2O_2}) \approx nM = 5.5\times 10^{-5}\times 34 \approx 1.9\times 10^{-3}\ \mathrm{g}=1.9\ \mathrm{mg}$$
解釈:この仮定だと「数ジュール」の熱で十分で、そのための過酸化水素は数 mg という見積もりになります。
反応室が“局所・少量”だから、熱が効きやすい。さらに蒸気ができると、その膨張が圧力源になります。
注意:実際は混合物であり、反応室の壁への熱損失、生成ガスの仕事、噴射に乗る運動エネルギーなどが入るため、
この計算は「見積もりの入口」です。けれど桁感としては、噴射の成立をイメージするには十分な足場になります。
図(反応)で“熱源”を押さえて、式(熱収支)で“使い道”を押さえる。
これで「100℃」に釣られずに済むたい。
なるほど…。“反応式(何が熱を出すか)”と“熱収支(熱がどこへ行くか)”が揃うと、
説明が一気に安定するのね。これは強い。
6) 圧力ができる:ガス+蒸気が体積を押し広げる
反応室では、過酸化水素の分解などによる酸素生成と、加熱による水蒸気の増加が同時に起こり得ます。
ガスのモル数が増えれば、同じ体積に押し込められるので圧力源になります。
圧力が立つと、噴射口(狭い流路)で速度へ変換され、スプレーとして外に出ます。
ここでの直感は「ガスが増える=圧力が上がる」ですが、もう一段だけ丁寧に言うなら、
液滴と蒸気の“二相”で出ることが重要です。
蒸気は膨張で押し出す役、液滴は刺激性成分を運ぶ役。
役割が分かれているから、少ない量でも効きます。
7) 連射っぽく見える理由:パルス(周期的噴射)を作る“圧力の上下”
見た目は連続噴射でも、実際は短いパルスの連なりとして説明されることがあります。
圧力が上がる→排出される→圧力が下がる→再び供給される、という
“圧力の上下”が繰り返されると、ジェットはパルスになります。
ここは「反応が一発で終わる」よりも、「反応と排出が噛み合って刻まれる」と見る方が自然です。
いわば反応室が、圧力をためて放つという動作をしている。
“虫サイズの圧力制御”と読めるところです。
連射っぽいの、かっこよかろ。虫サイズの“パルスジェット”たい。
その言い回しでまた調子に乗るのよ……。
でも“圧力の上下で刻む”って説明は、読者にも効くわね。
8) 「じゃあ虫は熱くないの?」:設計の要点は“局所化”と“排熱(排出)”
この疑問は正しいです。もし体全体が長時間高温なら、生体として成立しにくい。
そこで効くのが、さっきの前提――局所・短時間です。
反応は小さな反応室に閉じ込め、生成した熱は蒸気と一緒に外へ出す。
つまり「熱を溜め込む」のではなく、「熱を運んで外へ捨てる」設計になっています。
工学的に言えば、反応室は熱源であると同時に、噴射という排出手段(排熱手段)を持つ。
自分を守るための噴射が、同時に自分を守るための排熱になっている。
ここまで見えると、「すごい虫」で終わらずに“構造として理解できた感”が残ります。
9) 自由エネルギーの言葉で仕上げる:反応が“進みたがる”から成立する
反応が自発的に進むかは、ギブズ自由エネルギー変化 $ \Delta G $ が効きます。
ざっくり言うなら、$ \Delta G < 0 $ の反応は“進みたがる”。
そして、反応の“熱っぽさ”はエンタルピー変化 $ \Delta H $ が効きます。
$$\Delta G = \Delta H – T\Delta S$$
ミイデラゴミムシの仕組みは、進みたがる反応を、必要な瞬間だけ混ぜて一気に進めることで、
反応熱とガス発生を“圧力と噴射”に変換している、と見るのが一番すっきりします。
うん、納得。図で「何が熱源か」を押さえて、計算で「どのくらいの熱が要るか」を掴めた。
もう“100℃の数字”に振り回されないで説明できる。
そうたい。結局は「熱を作って、圧力にして、外へ出す」だけたい。
一本筋が見えたら、話は安定するけんね。
テンプレ
まずは“熱収支1本”で、現象を分解する。
反応熱で相変化が起きて噴射につながる現象は、細部が違っても同じ型で整理できます。
ここでは“考える順番”だけ固定します(数字は後からでOK)。
(1)系の範囲を決める
「どこで反応が起きるか」「どこから外へ出るか」を線で囲む。
短時間なら断熱近似(外へ逃げる熱を無視)から始める。
(2)反応熱を $Q$ と置く
$$Q \approx -\Delta H_\mathrm{rxn}\,n_\mathrm{lim}$$
$n_\mathrm{lim}$ は不足側(律速側)の物質量。符号は “出る熱を正” に揃えると見通しが良い。
(3)顕熱と潜熱に割る
$$Q \approx m\,c_p\,(T_b – T_0) + m_v\,L_v$$
まず $T_b$(沸点)に届くか。届いたら温度の伸びは鈍って、蒸気量 $m_v$ が増えやすくなる。
(4)圧力→流速の変換を見る
蒸気・反応ガスが増えるほど圧力源になる。最後に噴射口(流路)で速度に変換される、と繋げる。
(5)“反応の見取り図”を先に置く
「何が酸化され、何が還元され、何が増えるか」を図か代表式で示す。
これだけで“熱源がどこか”が見えるようになる。
落とし穴
“100℃”を、万能の真実みたいに扱う。
落とし穴はこれ一つ。数字を固定してしまうことです。
噴射は小さく、二相流で、混合物で、外気で急冷される。
だから温度の定義(どの位置の、どの相の、どのタイミングの温度か)を曖昧にすると、
途端に議論が破綻します。
回避策は簡単で、「温度の一点勝負」をやめて、
熱収支(顕熱+潜熱)→ 圧力 → 噴射の因果で語ること。
そうすると、温度が多少揺れても説明が崩れません。
締め
“図”と“熱収支”が揃うと、説明が強くなる。
今日は「反応の見取り図(何が熱源か)」と「熱収支(熱がどこへ行くか)」をセットにしたけんね。
これができたら、“数字だけの話”にならん。
うん。図が入ったことで、説明がすごく自然になった。
“反応で熱が出る→沸騰と蒸気→圧力→噴射”って、ちゃんと一本で言えるわ。
じゃあ次からは“高温二相噴射現象”って呼ぶたい。……言葉だけ急に賢くしても、バレるか?
そういうとこよ……。でも今日は許す。内容がちゃんと良いから。
出典
・古典的報告(「100℃」で引用される入口):PubMed: Biochemistry at 100°C: Explosive Secretory Discharge of Bombardier Beetles
・モデル化による仕組みの整理(温度・圧力・流れの見方):PMC: A mathematical model of the defence mechanism of a bombardier beetle
・物性・熱化学の代表値(比熱・蒸発潜熱・反応熱の参照先):NIST Chemistry WebBook